
Структура хроматина
Химический состав хроматина был установлен несколько лет назад. Однако функции его составных частей, способ их организации, механизм конденсации хроматина во время митоза и последующего разрыхления, способ, с помощью которого происходит экспрессия определенных генов в клетках какого-либо типа и репрессия в других, механизм экспрессии генов в определенные периоды жизни и их репрессии в другое время стали проясняться лишь недавно. Для того чтобы понять механизм экспрессии генов и способы его регулирования, необходимо знать структуру и организацию хроматина.
Тщательные биохимические и биофизические исследования с использованием электронной микроскопии, начатые в 1973 г., позволили установить структуру и функции хроматина. Когда хроматин тимуса теленка гидролизовали ДНКазой, появлялись частицы размером 200 пар оснований или кратным ему [157]. Это свидетельствует о том, что хроматин имеет повторяющиеся участки. Олинс и Олинс [272] выдерживали интерфазные ядра тимуса и печени крысы и эритроциты цыпленка в гипотонической среде и изучали их под электронным микроскопом после соответствующего окрашивания. Хроматин выглядел как цепочка бусинок диаметром 7 нм, связанных друг с другом тяжами ДНК диаметром 1,5 нм (рис. 2.2). Одновременно было показано [163], что при расщеплении хроматина микрококковой или стафилококковой нуклеазами, которые разрывают обе цепи ДНК, образуются частицы диаметром 7 нм, содержащие 200 пар оснований. В работе с использованием биохимических методов и дифракции рентгеновских лучей [200] также установлено, что частицы, получаемые в процессе расщепления нуклеазой, содержат 200 пар оснований ДНК; это составляет почти 85% общего содержания ДНК в хроматине. Каждая из этих частиц содержит по две молекулы гистонов Н2А, Н2В, Н3 и Н4, образующих октамер. Таким образом, эти частицы, позднее названные нуклеосомами [139], содержат восемь молекул гистонов и 200 пар оснований ДНК. Показано также [139], что при соединении гистонов четырех типов и ДНК появляются частицы, похожие на те, которые образуются из хроматина после расщепления нуклеазой. Гросс-Беллард и Шамбон ([139] высказали предположение, что центральную роль в формировании нуклеосомы играют богатые аргинином гистоны Н3 и Н4. Гистон Н1 отсутствует в этих частицах, он расположен между нуклеосомами.
![Рис. 2.2. А. Электронная микрофотография хроматина из Oncopeltus fasciatus. В областях, свободных от волокон рибонуклеопротеида, виден хроматин в виде бусин; × 67000 [120]. Б. Схематическое изображение структуры хроматина](pic/000014.jpg)
Рис. 2.2. А. Электронная микрофотография хроматина из Oncopeltus fasciatus. В областях, свободных от волокон рибонуклеопротеида, виден хроматин в виде бусин; × 67000 [120]. Б. Схематическое изображение структуры хроматина
На основе описанных выше исследований было высказано предположение [198], что основная структура хроматина состоит из повторяющихся частей, содержащих октамеры гистонов четырех типов и 200 пар оснований ДНК. Во всех изученных до сих пор организмах соотношение количества ДНК и гистонов равно приблизительно 1 и везде имеются повторяющиеся участки октамеров гистонов, связанных приблизительно с 200 парами оснований ДНК, которые образуют линейную цепь нуклеосом диаметром 10 нм. Количество ДНК в нуклеосомах различных органов и организмов варьирует от 140 до 240 пар оснований [116]. Межнуклеосомная, или линкерная, ДНК более чувствительна к микрококковой нуклеазе, а нуклеосомная ДНК - к панкреатической ДНКазе I. Микрококковая нуклеаза и ДНКаза I и II расщепляют находящуюся внутри нуклеосомы нуклеосомную ДНК (или ДНК сердцевины), образуя фрагменты ДНК длиной 10 пар оснований или кратные им, но разрывают ее в разных местах [329]. Когда нуклеосомы из разных тканей и организмов расщепляют микрококковой нуклеазой, чтобы удалить линкерную ДНК, получают стабильные нуклеосомы с мол. массой 200000 и коэффициентом седиментации 11S, содержащие октамер гистонов и ДНК длиной 140 пар оснований [328]. Таким образом, размер ДНК, входящей в состав нуклеосомы, у всех организмов одинаков. Длина межнуклеосомной, или спейсерной, области, которая разделяет соседние нуклеосомы, зависит от функционального состояния хроматина. Транскрипционно активный хроматин имеет укороченную спейсерную область [225, 262].
При определении местоположения гистонов и ДНК в нуклеосомных мономерах хроматина тимуса теленка с помощью метода ЯМР было показано, что радиусы вращения ДНК и белка составляют 5 и 3 нм соответственно. Это свидетельствует о том, что ДНК расположена вне гистоновой сердцевины [21]. Внутренняя белковая сердцевина нуклеосомы имеет диаметр 6,4 нм; она окружена оболочкой из ДНК толщиной 2 нм, так что общий диаметр нуклеосомы составляет 10,4 нм. Эти данные были подтверждены иммунологическими исследованиями. Ни одна из сывороток против четырех гистонов, кроме анти-Н2В, не реагирует с нуклеосомой [2]. Это доказывает, что только гистон Н2В взаимодействует со своим антителом.
В растворе гистоны разных типов связываются попарно [94], причем наиболее сильная связь наблюдается между гистонами Н3 и Н4. Нуклеосома имеет ось симметрии второго порядка. В детальных рентгеноструктурных и электронно-микроскопических исследованиях кристаллических препаратов нуклеосом [117] показано, что сердцевина нуклеосомы представляет собой плоский клинообразный диск размером 5,7×11×11 нм. Полагают [117], что 140 пар оснований ДНК составляют 1,75 витка спирали, диаметр витка равен 9 нм, а его шаг - 2,8 нм (рис. 2.3). Это соответствует приблизительно 80 парам оснований на сверхспиральный виток В-формы ДНК. Гистоны частично погружены в большую бороздку ДНК, а малая бороздка остается открытой. Брем [50] считает, что сердцевина нуклеосомы имеет клинообразную форму, ее размеры 5,5×10×12 нм, а 140 пар оснований ДНК расположены в виде витка. Длина 140 пар оснований ДНК в 6-7 раз превышает размеры нуклеосомной сердцевины. Таким образом, ДНК конденсирована в 6-7 раз, что обусловлено ее связыванием с основными участками цепей восьми молекул гистонов и закручиванием вокруг сердцевины сверхспирали [337]. Это обеспечивает защиту нуклеосомной ДНК от микрококковой и стафилококковой ДНКаз. Однако панкреатическая ДНКаза I расщепляет эту ДНК с образованием фрагментов, состоящих из десяти нуклеотидов. Из-за спиральной структуры ДНК разные участки ее цепи отличаются друг от друга по чувствительности к ДНКазе I [238]. По-видимому, внутри нуклеосомы имеются отдельные центры, по которым происходит расщепление под действием ДНКазы. ДНКаза II расщепляет нуклеосомную ДНК с образованием двух фрагментов по 100 пар оснований [15]. С помощью гидродинамических методов показано [135], что нуклеосома претерпевает два конформационных перехода, зависящих от концентрации соли. Это служит дополнительным доказательством того, что нуклеосома включает две субчастицы, или половины.
![Рис. 2.3. Предполагаемое закручивание суперспирали ДНК вокруг сердцевины нуклеосомы. Отмечены места расщепления ДНК нуклеазой [117]](pic/000015.jpg)
Рис. 2.3. Предполагаемое закручивание суперспирали ДНК вокруг сердцевины нуклеосомы. Отмечены места расщепления ДНК нуклеазой [117]
Сердцевина нуклеосомы содержит по две молекулы каждого из Н2А-, Н2В-, Н3- и Н4-гистонов, которые образуют октамер. Положительно заряженные вытянутые цепи этих гистонов электростатически связаны с отрицательно заряженной ДНК. Полагают, что четыре гистона расположены относительно ДНК следующим образом:
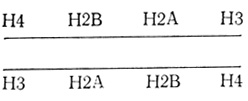
Два гистона, Н3 и Н4, богатые аргинином, вероятно, взаимодействуют с двумя концами фрагмента ДНК. Когда эти гистоны добавляют к двухцепочечной ДНК, они образуют характерную структуру типа бублика, видимую в электронный микроскоп [129]. При воссоединении гистонов сердцевины со 140 парами оснований ДНК образуются частицы, имеющие тот же самый коэффициент седиментации, что и нуклеосомы, полученные из хроматина [36, 345]. Было также показано, что одни гистоны Н3 и Н4 образуют с ДНК структуры, похожие на сердцевины нуклеосом, устойчивые к трипсину [64, 327] и дающие картину дифракции рентгеновских лучей, похожую на картину для нативных нуклеосом [261]. Когда гистоны Н3 и Н4 добавляют к ДНК, они связываются со 140 парами оснований ДНК, которая имеет 1,5 сверхспиральных оборота вокруг тетрамера [195]. Образующаяся структура представляет собой цилиндр с размерами 45×8×8 нм. При последующем добавлении гистонов Н2А и Н2В цилиндр сжимается и становится похожим на нативную нуклеосому. Аналогичные явления наблюдал Картер [70]. Это согласуется с высказанным ранее [198] предположением, что гистоны Н3 и Н4 играют существенную роль в образовании структуры нуклеосомы. Эти два гистона наиболее консервативны, содержат большое количество β-структур и взаимодействуют друг с другом сильнее, чем с другими гистонами. По степени связывания с ДНК гистоны располагаются в следующем порядке: Н3 и Н4>Н2А>Н2В>Н1 [283]. При изучении поперечных сшивок показано, что связаны следующие пары: Н3-Н4, Н2А-Н2В и Н2В-Н4 [84].
Согласно одной из точек зрения, сначала 2 молекулы гистона Н3 и 2 молекулы гистона Н4 образуют тетрамер и связываются со 140 парами оснований ДНК, формируя основную сердцевину нуклеосомы. На втором этапе в эту структуру включаются по две молекулы гистонов Н2А и Н2В, чем и завершается образование нуклеосомы [42, 64, 258, 372]. При изучении сборки новореплицированного хроматина Drosophila показано, что гистоны Н3 и Н4 соединяются с ДНК в течение или вскоре после ее синтеза, гистоны Н2А и Н2В - на 2-10 мин позже, а гистон Н1 - через 10-20 мин, и в результате образуется зрелый хроматин [375]. По-видимому, во взаимодействие с ДНК вовлечены COOH-концы четырех гистонов, так как удаление ЫН2-концевых участков цепей гистонов не влияет на структуру нуклеосомы [371]. Гистоны Н2А и Н2В образуют димеры, взаимодействуя своими центральными неполярными областями, так что NH2- и COOH-концы остаются свободными. Гистоны Н3 и Н4 образуют димеры путем образования связей между их центральными неполярными областями и COOH-концами, так что основные NH2-концевые области нуклеосомных гистонов доступны для взаимодействия с кислотными группами ДНК [72]. Роль NH2-концевых областей четырех гистонов пока не установлена, хотя известно, что они связываются с ДНК. Мирзабеков и др. [252] путем ковалентных сшивок гистонов с 5′-концевыми фрагментами ДНК показали, что каждый гистон связан с 10 парами оснований ДНК. Сборка нуклеосом, по-видимому, контролируется НГБ. Так, очищенный препарат этих белков, выделенный из яиц Xenopus laevis, в бесклеточной системе в присутствии гистонов и очищенной ДНК катализирует образование нуклеосом [217].
Таким образом, основная структура хроматина представляет собой цепь линейно расположенных нуклеосом диаметром 10 нм, которую называют нуклеосомной фибриллой. Это низший уровень организации хроматина. Структуру более высокого порядка образуют нуклеосомы, свернутые в спираль, которая имеет диаметр 20-30 нм и шаг 10 им. Свертывание нуклеосом в спираль, по-видимому, обеспечивается богатым лизином гистоном Н1, который, как было показано, соединяется с линкерной ДНК между соседними нуклеосомами. Этот вывод следует из того, что после расщепления мононуклеосом стафилококковой нуклеазой размер ДНК уменьшается с 200 до 140 пар оснований, причем одновременно освобождается 35-парный фрагмент ДНК, связанный с гистоном Н1 [20]. Когда гистон Н1 добавляли к хроматину, который был его лишен, увеличение сродства к нему наблюдалось только до стадии образования октануклеосомы, но не далее [301]. Связывание с гистоном Н1 не только стабилизирует ДНК в линкерной области, но вызывает также ее дальнейшую конденсацию и свертывание [75]. Более высокий порядок структуры хроматина (по сравнению с цепочкой бусин) представляет собой спираль из частиц октануклеосом, образование которой обеспечивается гистоном Н1 или гистоном Н5 (в случае эритроцитов, содержащих ядра). Это согласуется с результатами, согласно которым полинуклеосомы, содержащие около шести нуклеосом, являются, по-видимому, основными матрично активными единицами хроматина, связывающимися с эндогенной РНК-полимеразой [344]. Олигонуклеосомы служат лучшими матрицами для транскрипции, чем мононуклеосомы, и на них синтезируются более длинные транскрипты [318].
Нуклеосома - динамическая единица как в структурном, так и в функциональном отношении. Как сказано выше, она состоит из двух половин, что может быть определено путем специфического связывания восьми молекул гистонов с ДНК. То, что нуклеосомы в транскрипционно активном состоянии подвержены конформационным изменениям, становится очевидным при изучении их чувствительности к ДНКазе I. Этот фермент преимущественно воздействует на те последовательности ДНК, которые активно транскрибируются. Он удаляет ДНК, кодирующую глобин, из ядер эритроцитов цыпленка, но не действует на ядра клеток мозга или фибробластов [125, 282, 367]. На ДНК яичного альбумина эритроцитов и фибробластов, в которой этот ген не транскрибируется, фермент также не действует. Стафилококковая нуклеаза, которая, как известно, расщепляет ДНК в межнуклеосомной области, не расщепляет ДНК глобина из эритроцитов цыпленка. Если мономерные нуклеосомы, полученные из этих клеток действием стафилококковой ДНКазы, обработать затем ДНКазой I, то преимущественно удаляются гены глобина. Показано [125], что ген яичного альбумина предпочтительно расщепляется ДНКазой в клетках яйцевода курицы и не расщепляется в других клетках, в которых он не транскрибируется. В клетках хомяка, трансформированных аденовирусом, последовательности ДНК аденовируса, которые легко расщепляются ДНКазой I, представляют собой участки, с которых транскрибируется мРНК. Другие вирусные последовательности резистентны к этой нуклеазе [119]. Из приведенных наблюдений следует, что во время транскрипции происходят конформационные изменения в хроматине, так что ДНК становится более чувствительной к ДНКазе I, но ее чувствительность к стафилококковой нуклеазе остается прежней. Полученные результаты подтверждаются данными электронной микроскопии [313]. Показано, что в процессе развития ооцитов трех видов Xenopus транскрипционно активный ядрышковый хроматин выглядит гладким, нуклеосомы в нем присутствуют в небольшом количестве или вообще отсутствуют. Неактивный хроматин имеет вид бусин. Пониженная транскрипционная активность хроматина коррелирует с появлением бусин в его структуре, тогда как транскрипционно активный хроматин содержит больше мононуклеосом, чем транскрипционно неактивный, что и означает увеличение той области хроматина, которая активна при транскрипции [223]. Электронно-микроскопическое изучение активно транскрибируемых рибосомных генов Physarum polycephalum показывает, что ДНК в транскрибируемом участке имеет вытянутую конформацию [179]. Таким образом, структура хроматина и, в особенности, нуклеосом подвержена конформационным изменениям в процессе транскрипции, а возможно, и репликации. Не исключено, что это вызвано связыванием с НГБ. Для ковалентной модификации гистонов различных типов, па-пример фосфорилирования, ацетилирования, метилирования и ADPрибозилирования, необходимы эффекторы.
|
ПОИСК:
|
© GELIB.RU, 2013-2019
При использовании материалов проекта обязательна установка активной ссылки:
http://gelib.ru/ 'Геронтология и гериатрия'
При использовании материалов проекта обязательна установка активной ссылки:
http://gelib.ru/ 'Геронтология и гериатрия'